terça-feira, 26 de julho de 2016
domingo, 17 de julho de 2016
Hernia de hiato, esofagite
esofagite
A esofagite desenvolve-se quando a frequência destes episódios, ou o volume do refluxo aumenta além de um determinado ponto, ou quando o esôfago é incapaz de limpar imediatamente o material refluído. A inflama- ção agrava-se em relação direta com o intervalo de tempo em que o esôfago fica exposto ao material refluído. A esofagite, que geralmente fica limitada a 7 a 10 cm distais do esôfago, é causada, principalmente, por ácido e pepsina. No entanto o esôfago é sensível aos ácidos biliares, os quais podem desempenhar um papel, principalmente, nos pacientes com operação gástrica prévia2
Três anormalidades do esfíncter permitem o refluxo nos pacientes com esofagite: 1-relaxamentos transitórios do esfíncter na presença de pressão normal em repouso; 2-refluxo espontâneo na presença de pressão em repouso baixa; 3-aumentos transitórios da pressão intra-abdominal que superam uma pressão do esfíncter em repouso baixa. Três quarto dos episódios de refluxo nos pacientes com esofagite seguem um relaxamento esfinctérico transitório.
. O refluxo noturno está relacionado com a frequência aumentada de relaxamento transitório do esfíncter e associado a surtos periódicos de motilidade gástrica aumentada. A possibilidade de desenvolver esofagite é maior durante a noite, porque o material refluído é principalmente composto de ácido e pepsina, a peristalse esofágica está diminuída, e existe menos saliva disponível para neutralizar o ácido. À medida que a inflamação da parede esofágica se agrava, a peristalse é adicionalmente comprometida, provocando a expansão e lesão adicionais pelo ácido esofágico
As características histopatológicas da esofagite por refluxo ácido incluem hiperplasia epitelial, balloon cels, hiperplasia de células basais, alongamento papilar, dilatação dos espaços intercelulares representando edema epitelial, congestão vascular e infiltração de células inflamatórias que incluem linfócitos, neutrófilos e eosinó- filo
• Estreitamento do esôfago (estenose esofágica): Danos às células do esôfago inferior pela exposição prolongada ao ácido pode levar à formação de tecido cicatricial. O tecido cicatricial estreita a via alimentar, causando dificuldade de deglutição. • Esôfago de Barrett: A exposição ao suco gástrico por vários anos pode levar à transformação do revestimento normal do esôfago em um revestimento diferente, com células intestnalizadas, que recebe o nome de Esôfago de Barrett.
Tabela 1. Classificação de Los Angeles da Esofagite
A Uma ou mais quebras de mucosa menores do que 5 mm, que não se estendem entre duas pregas longitudinais. B Uma ou mais quebras de mucosa maiores do que 5 mm em sua maior extensão, não contínuas entre os ápices de duas pregas esofágicas. C Quebras de mucosa contínuas (ou convergentes) entre os ápices de pelo menos duas pregas, envolvendo menos do que 75% do órgão. D Quebras de mucosa ocupando mais de 75% da circunferência do órgão




Lesões cáusticas
Classificação das lesões corrosivas em esôfago
(Zargar modificada)
Grau 1
Edema e eritema de mucosa;
Grau 2a
Friabilidade, erosões, eritema severo, exsudato inflamatório, ou erosões superficiais;
Grau 2b
Grau 2a com úlceras profundas ou circunferenciais;
Grau 3a
Áreas com necrose, com coloração marrom, acinzentada ou enegrecida, ulcerações profundas;
Grau 3b
Necrose extensa.
TRATAMENTO
1) Alterações nos hábitos de vida
– Elevação da cabeceira da cama. Pode-se colocar algum livro ou bloco em baixo dos pés da cama para se elevar a cabeceira em uns 20 cm. Pessoas com EEI incompetente apresentam piora do refluxo ao deitar, quando a gravidade já não mais dificulta o conteúdo gástrico de alcançar o esôfago.
– Não se deitar por pelo menos 1,5 a 2h após as refeições. Evite comer grandes quantidades de uma só vez. Quanto mais cheio fica o estômago, maior o risco de refluxo.
– Alguns alimentos pioram os sintomas de quem tem DRGE, entre eles: álcool, refrigerantes, frituras, pimenta, chocolate, sucos cítricos e molho de tomate.
– Evitar cigarro
– Mastigar chicletes após as refeições reduz os sintomas em alguns pacientes.
2) Medicamentos para refluxo
Aqueles com sintomas moderados ou nos quais as medidas educacionais não surtiram efeito devem ser tratados com medicamentos a fim de impedir uma esofagite mais grave e o aparecimento do esôfago de Barret.
Os inibidores da bomba de prótons são drogas que diminuem a secreção de ácido pelo estômago, diminuindo assim o risco de lesão do esôfago naqueles com refluxo. Os mais conhecidos são: Omeprazol, Lansoprazol e Pantoprazol (leia: OMEPRAZOL – PANTOPRAZOL – LANSOPRAZOL). A Ranitidina pertence a outra classe de drogas, mas também reduz a acidez estomacal, porém, sua potência é inferior a dos inibidores de bomba. O tempo mínimo de tratamento é de 8 semanas.
3) Cirurgia para refluxo
A cirurgia para restabelecer a competência do EEI pode ser necessária nos pacientes que não respondam as medidas acima e mantenham sintomas intensos. Doentes com esofagite grave, estenose do esôfago ou com esôfago de Barrett também são candidatos à cirurgia.
a. Entretanto, algumas complicações e falhas têm sido descritas no pós-operatório dentre elas a estenose da junção esofagogástrica, a disfagia devido à hiatoplastia muito “apertada” ou fundoplicatura realizada com o corpo gástrico ou ainda migração da fundoplicatura para o tórax por deiscência da hiatoplastia. Além disto, pode ocorrer a recidiva do refluxo gastroesofágico, consequente à migração da válvula com deiscência total ou parcial de suturas. Contudo, nem sempre estas alterações anatômicas pós-operatórias apresentam sintomas típicos.
Após a correção cirúrgica laparoscópica ou convencional do refluxo gastroesofágico algumas queixas são comuns, como distensão pós-prandial, dificuldade de eructar e vomitar, e às vezes, disfagia. Na maioria dos casos de disfagia o sintoma é intermitente e tende a desaparecer em até 30 dias após o procedimento, sem necessidade de tratamento específico ou nova intervenção cirúrgica. Porém, no caso de disfagia persistente, principalmente quando associada à perda de peso ou de disfagia importante também a líquidos, deve ser realizada investigação diagnóstica minuciosa. Esta disfagia persistente ocorre em aproximadamente 3% dos casos após o tratamento cirúrgico da DRGE por videolaparoscopia. Este quadro costuma levar à perda da qualidade de vida, emagrecimento e evidentemente muita insatisfação por parte dos pacientes operados

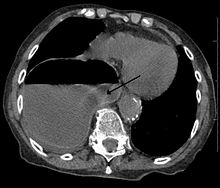
hernia de hiato
A hérnia de hiato é o deslizamento do estômago em direção ao esôfago, sendo que esta alteração anatômica ocorre devido à diferença entre a alta pressão dentro do abdome em relação à baixa pressão dentro do tórax.

Hérnia de hiato é a migração de parte do estômago (em casos mais sérios até do estômago todo) em direção do tórax. Esta migração ocorre pelo orifício natural existente no diafragma, chamado hiato – daí o nome hérnia de hiato. A hérnia muda a dinâmica da transição esofagogástrica, diminuindo sua capacidade de conter o refluxo, então, é muito comum a associação de hérnia de hiato com refluxo gastroesofágico.
A hérnia hiatal por deslizamento (imagem do meio) é a mais comum e corresponde a 95% dos casos.


La hernia hiatal gigante (HHG) con estómago intratorácico es una enfermedad poco frecuente. Durante el último tiempo hemos visto casos con mayor frecuencia en pacientes añosos y obesos. Habitualmente estas hernias se asocian a rotación gástrica órgano-axial, y pueden presentar complicaciones como vólvulo, perforación u obstrucción gástrica.

En la literatura, las hernias hiatales están clasificadas en 4 categorías(4,5):
* Tipo 1: Corresponde a la hernia hiatal por deslizamiento. La unión esófago-gástrica está desplazada hacia el tórax, debido a debilidad y elongación de la membrana frénico-esofágica. Constituye el 95% de todas las hernias hiatales.
* Tipo 2: Corresponde a la hernia hiatal paraesofágica. Existe un defecto focal, generalmente en el aspecto antero-lateral de la membrana frénico-esofágica. El cardias y la unión esófago-gástrica permanecen por debajo del diafragma. El fondo gástrico usualmente encabeza la herniación, pero todo el estómago puede migrar hacia cefálico, constituyendo un estómago intratorácico.
*Tipo 3: Es una hernia hiatal mixta, con componente por deslizamiento y paraesofágico. Habitualmente es una hernia grande, asociada a rotación gástrica.
* Tipo 4: Es una hernia tipo 3, que además posee herniación de otras estructuras abdominales, como colon, omento, intestino delgado o hígado.
Una hernia hiatal gigante es aquella que incluye al menos el 30% del estómago en el tórax(6). La mayoría de las veces, estas hernias corresponden a una hernia hiatal tipo 3, con componente por deslizamiento y paraesofágico(6).
A medida que el estómago se hernia hacia el tórax, éste va rotando. Más de dos tercios de las rotaciones gástricas se encuentran asociadas a hernias diafragmáticas(7-9). La rotación más común es la rotación anterior órgano-axial, donde el estómago rota a lo largo de su eje longitudinal, con movimiento hacia anterior y luego hacia cefálico de la curvatura mayor(4,7,10). El estómago también puede rotar en forma mesenterio-axial, es decir, en un eje perpendicular a su eje longitudinal, con movimiento hacia anterior y luego hacia la izquierda del antro
El tratamiento de los pacientes sintomáticos con hernia hiatal gigante con estómago intratorácico es quirúrgico. En caso de complicaciones, como vólvulo, obstrucción o perforación, la cirugía debe ser de urgencia. El abordaje quirúrgico puede ser a través del tórax o el abdomen(4). La cirugía laparoscópica puede ser usada tanto para hernias con rotación gástrica órgano-axial como mesenterio-axial
Esôfago - Anatomia
 Esôfago
EsôfagoO esôfago entra no tórax no nível da incisura esternal e sai em direção ao abdome ao nível de T10 ou T11. Ele está localizado no mediastino posterior cujos limites são o pericárdio e a traqueia anteriormente, as pleuras lateralmente e as vértebras posteriormente. O eixo do esôfago é ligeiramente curvado para a direita no tórax.
Não há variação na anatomia considerada normal. No entanto, seu eixo pode ser alterado perante a determinadas doenças como a acalásia em estágio avançado, levando ao maior risco de lesão pleural durante esofagectomia, especialmente do lado direito 11. Recentemente, alguns estudos mostraram também mudança no eixo anteroposterior do esôfago devido ao encurtamento dele consequente a estágios avançados de cifose 22


Pleura
As linhas da pleura parietal cobrem ambas cavidades torácicas e mediastino formando uma parede lateral.
Um recesso alongado da pleura penetra entre o esôfago e a veia ázigos no lado direito logo abaixo das veias pulmonares, em íntimo contato com o lado direito do esôfago, como observado em imagens de alta resolução de ressonância magnética. Este recesso tem implicações clínicas, pois podem estar associados com maior chance de danos pleurais durante a dissecção do esôfago mediotorácico.
Distalmente, a pleura esquerda está mais próxima do esôfago. Devido a isso, as perfurações esofágicas distais geralmente drenam para o espaço pleural esquerdo e a pleura esquerda é mais frequentemente lesada durante operações de esôfago distal

Aorta
O esôfago tem relação estreita com a aorta descendente e seu arco. Ele, envolto pelo arco da aorta, situa-se em posição anterolateral direita superiormente, torna-se anterior, na parte inferior do peito e vai para à esquerda anterolateralmente na altura do diafragma.
As artérias esofágicas (quatro ou cinco em número), surgem de parede anterior da aorta 8. Elas ramificam em pequenos ramos antes de entrarem na parede esofágica de modo que a perda de sangue durante a esofagectomia transhiatal é mínima e a hemostasia pode ser conseguida facilmente na medida em que são dissecados da parede esofágica 18.
Variações dos ramos do arco aórtico não são muito raras e podem estar presentes na população adulta (Figura 1). Arco aórtico direito pode tornar a esofagectomia mais difícil, especialmente a dissecação dos linfonodos paratraqueais direitos6. Pacientes com câncer de esôfago são submetidos rotineiramente à tomografia computadorizada do tórax e as variações da aorta e seus ramos podem ser diagnosticadas antes da operação. Nesse caso, toracotomia esquerda, ao invés de direita, é a via de escolha6, por vezes associada à esternotomia mediana16. Artérias subclávias com variações também estão em risco de lesão durante esofagectomia19.
Disfagia lusória é causada pela compressão vascular do esôfago. Ele tem sido descrito após as seguintes variações anatômicas: artéria subclávia direita ou esquerda que cruzam entre o esôfago e a coluna vertebral em 80% dos casos; em 15% dos casos, correm entre o esôfago e traquéia, e em 5% passam anteriormente tanto da traqueia como do esôfago, ou anéis vasculares, como em um ligamento arterioso esquerdo17.
Não foram encontradas variações anatômicas nos cadáveres abordados.
Veia ázigos
A veia ázigos origina-se no abdome e entra no tórax através do hiato aórtico do diafragma, sobe pelo lado direito da coluna vertebral e na altura da quarta vértebra torácica se projeta anteriormente em direção ao esôfago e a raiz do pulmão direito, terminando na veia cava superior. No hiato aórtico, a veia ázigos juntamente com o ducto torácico, está posicionada do lado direito da aorta. No tórax, ela se situa sobre as artérias intercostais, do lado direito da aorta e do ducto torácico, e é parcialmente coberta pela pleura 8.
A veia hemiázigos também começa no abdome. Ela entra no tórax, através do pilar esquerdo do diafragma, ascende pelo lado esquerdo da coluna vertebral, na altura da vértebra torácica , passa sobre coluna, atrás da aorta, do esôfago e do ducto torácico, em direção a veia ázigos 8.
O veia hemiázigos acessória desce pelo lado esquerdo da coluna vertebral. Ela cruza o corpo da oitava vértebra torácica para se juntar a veia ázigos ou termina na hemiazigos 8.
A anatomia do sistema ázigos é de interesse durante a esofagectomia mesmo sendo retirada em bloco26. Alguns autores, no entanto, acreditam que a ressecção do sistema ázigos não é considerada essencial durante a esofagectomia radical. O sistema ázigos é abordado também para casos benignos para permitir melhor exposição do esôfago no mediastino proximal. Variações são incontáveis e se relacionam principalmente com a origem dos vasos ou a comunicação entre o lado esquerdo e direito do sistema 24 (Figura 2). No entanto, a importância clínica dessas variações é desprezível uma vez que elas podem ser prontamente reconhecidas e compreendem vasos de pequeno calibre, que podem ser facilmente ligados sem qualquer consequência. A maior parte das variações clínicas importantes ocorre na configuração da veia cava (superior ou inferior), tais como duplicação 7 e agenesia 2 total ou parcial, momento em que uma grande dilatação do sistema ázigos pode estar presente.

Nervo vago
Tradicionalmente, a anatomia cirúrgica do nervo vago foi de interesse para a cirurgia de úlcera péptica. Atualmente, os cirurgiões de esôfago estão preocupados com a preservação do vago durante uma esofagectomia, uma vez que parte das comorbidades no pós-operatório estão associadas com a vagotomia1.
Livros de anatomia clássicos descrevem o vago no mediastino como um plexo em torno da esôfago 8. Artigo anterior dos autores mostrou um ou mais troncos vagais bilateralmente em 30 dissecções13 (Figura 3). Curiosamente, esses troncos foram preservados após uma esofagectomia poupadora do vago realizada em cadáveres13.
Nervo laríngeo recorrente

O nervo laríngeo recorrente é o ramo mais importante do vago durante a esofagectomia. O direito origina-se na altura da artéria subclávia direita por trás da articulação esternoclavicular, forma um laço em torno da artéria e ascende ao pescoço28. O esquerdo origina-se na borda inferior do arco aórtico, forma um laço em torno dele e ascende ao pescoço 28. De cada lado, sobem por um sulco formado entre a traqueia e o esôfago, passa por baixo do bordo inferior do músculo constritor inferior da laringe e entra atrás do corno inferior da articulação da cartilagem tiróide com o cricoide 8.
O nervo recorrente pode ser facilmente danificado no seu curso pelo pescoço, devido à proximidade com o esôfago. No mediastino, o esquerdo apresenta risco ao nível do arco aórtico durante a linfadenectomia torácica na janela aortopulmonar ou paratraqueal. O nervo direito geralmente não encontra-se no campo operatório.
Vários estudos têm descrito a anatomia cirúrgica do nervo laríngeo recorrente no pescoço, uma vez que é grande preocupação durante a operação da tiróide. Há escassez de estudos relacionados com a anatomia do nervo laríngeo no tórax. Variações anatômicas, no entanto, são incomuns. Nervo laríngeo não recorrente foi relatado em menos de 1% dos casos 3, quando tem curso torácico e está automaticamente sob proteção contra ferimentos. É talvez associado à artéria subclávia variante ou anormalidades aorta. O nervo laríngeo recorrente pode ainda existir como dois feixes de um lado 2.
Em todos os 20 casos dissecados, o recorrente esquerdo surgia a partir do tronco do vago e envolvia o arco aórtico, próximo do ligamento arterioso. No lado direito, foram encontrados quatro padrões de variações anatômicas (Figura 4) - tipo 1: não recorrente - dois casos (10%), nervo laríngeo surgia a partir do tronco vago; tipo 2: recorrência na artéria subclávia - três casos (15%), surgia a partir do tronco vago e retornava após envolver a artéria subclávia; tipo 3: reincidência no tronco braquiocefálico - 12 casos (60%), surgia a partir do tronco vagal e voltava ao redor do tronco braquiocefálico, tipo 4: duplicação ou triplicação - em dois casos (10%) surgia a partir do tronco vagal e tinha dois ramos, um voltava ao redor do tronco braquiocefálico e outro ao redor da artéria subclávia; e um (5%) surgia a partir do tronco vagal com três ramos, uma volta ao redor do tronco braquiocefálico e duas voltas ao redor da artéria subclávia.

Ducto torácico
Origina-se na parte cranial no abdome na cisterna do quilo. Com a aorta à sua esquerda e veia ázigos à direita, ele passa através do hiato aórtico do diafragma. Mantém essa relação à medida que passa através do mediastino posterior. As vértebras torácicas, certas artérias intercostais, porções terminais da hemiázigos e das veias acessórias hemiázigos são posteriores ao ducto torácico; já o esôfago, diafragma e pericárdio são anteriores. No nível de T7, o ducto torácico percorre obliquamente atrás do esôfago até ao nível da quinta vértebra torácica. Em T5, ele reaparece posterior ao esôfago para continuar sua jornada para subir, à esquerda do esôfago e ficar medial à pleura até o pescoço 8. As variações são muito comuns em seu final quando se encontra no pescoço 25.

Jacobsson em 1972 14 investigou 122 casos de autópsia para estudar a anatomia e patologia do ducto torácico. O ducto torácico inicia abaixo do diafragma e passa através do mediastino posterior. Em 1% é estrutura completamente plexiforme por todo percurso. Suas variações principais (Figura 6) incluem ser duplo, triplo, unilateral esquerdo, terminar à direita ou bilateralmente, bem como mais raramente terminar na veia ázigos. Em alguns casos, os componentes abdominais do tronco podem subir cranialmente em ambos os lados ou apenas pela esquerda da aorta. Em mais da metade dos casos não ocorre apresentação típica do ducto 10.
O maior interesse na anatomia cirúrgica do ducto torácico durante esofagectomia é devido a possibilidade de lesão inadvertida e consequente quilotórax. A identificação intra-operatória da lesão e da conduta em si pode ser difícil. Ligadura em massa do ducto, incluindo todo o tecido entre a aorta, coluna, esôfago e pericárdio é recomendado por alguns autores em casos de suspeita de lesão. A ligadura de ducto é segura; um estudo randomizado mostrou diminuição significativa no quilotórax pós-operatório com ligadura de rotina. Ligadura em massa é preferível ser aplicada quando é identificada duplicação ou ducto plexiforme



Hernia diafragmática traumática
Entre as cavidades abdominal e torácica, há um gradiente de pressão que varia normalmente entre 7 e 22cmH2O, podendo atingir 100cmH2O durante a inspiração forçada máxima, quando a pressão interpleural é mais negativa1,3.5,6.
No trauma abdominal contuso grave, há um aumento de dez vezes na pressão abdominal, transmitindo subitamente a energia cinética através das cúpulas frênicas6. Qualquer porção do diafragma pode ser lesada, entretanto, a maioria das lacerações ocorre em direção radial na área póstero-lateral do diafragma esquerdo, que corresponde a um ponto embriológico de fraqueza.1,6. O centro tendíneo do diafragma, por ser inextensível, também é sede freqüente de lesões


A ruptura diafragmática ocorre em 0,8% dos pacientes vítimas de acidentes automobilísticos e em cerca de 3% a 5% dos casos de traumatismo abdominal fechado6,8.
Ocorre também após trauma penetrante (cerca de 13% a 19% projétil lesam o diafragma)5, tanto por arma de fogo (46%) como por arma branca (15%)
O impacto lateral no trauma contuso tem três vezes mais chance de resultar em ruptura diafragmática do que o impacto frontal, com tendência a ruptura ipsilateral do lado do impacto7. É rara a presença de hérnia diafragmática direita não associada a acidentes automobilísticos7

A hérnia diafragmática é definida como a evisceração transdiafragmática de conteúdo abdominal no torax3. Os órgãos abdominais mais frequentemente herniados através do defeito diafragmático são o estômago, omento, cólons e fígado5.

A hérnia diafragmática deve ser diferenciada da eventração diafragmática, que é uma elevação permanente da musculatura frênica devido a aplasia, paralisia ou atrofia, porém o diafragma mantém sua continuidade e inserção na margem costal, raramente produzindo sintomas e não requerendo tratamento
O sinal de Gibson, com o abdome escavado mostrando assimetria dos hipocôndrios é pouco encontrado8. A dificuldade de passagem do cateter nasogástrico na junção esofagogástrica é altamente sugestiva de lesão diafragmática com herniação do estômago para o tórax8 .
A região de transição toracoabdominal é a área compreendida anterior e superiormente pelos mamilos (4º espaço intercostal), posterior e superiormente, pela ponta da escápula (7º espaço intercostal) e, inferiormente, pelo rebordo costal. Esta área contém o diafragma durante a sua excursão nos ciclos respiratórios. Pacientes assintomáticos com ferimentos penetrantes nesta área devem ser investigados imediatamente para excluir lesão diafragmática5. A exploração local dos ferimentos não é recomendada pelo risco de induzir a um pneumotórax5,22.
A radiografia simples de tórax, geralmente revela as hérnias diafragmáticas agudas, mostrando um padrão de gás anormal acima do hemidiafragma com elevação e irregularidade, principalmente em casos de trauma contuso2,23. Nos casos de trauma penetrante é frequente o exame ser normal em 36% a 67% dos casos2,5,23(Figura 1). É importante a realização da radiografia de tórax em perfil, pela grande incidência de lesões diafragmáticas posteriores8. Outras características radiológicas em casos de hérnias diafragmáticas, menos freqüentemente encontrados, são: falha da radiografia de tórax retornar ao normal durante o tratamento com drenagem pleural e o hemotórax persistente
Como a presença de hérnia diafragmática pode determinar sinais e sintomas que sugiram a necessidade de drenagem torácica, é imperativo que se faça o diagnóstico correto, pelo risco de drenagem iatrogênica da víscera herniadas8. Para evitar tal complicação, o Advanced Trauma Life Support (ATLS) preconiza a drenagem pleural na linha mamilar entre a linha axilar média e anterior, sendo necessária a exploração do oríficio com o dedo indicador, antes da introdução do dreno pleural
A radiografia de tórax, usualmente, fornece o diagnóstico, mostrando mais comumente as seguintes anormalidades: elevação com irregularidade do hemidiafragma, padrão anormal de gás acima do diafragma com alças distendidas e cateter nasogástrica dentro do hemitórax2,23.
O uso de contraste radiológico pode ser feito tanto para diagnóstico de hérnias agudas quanto crônicas para documentar a posição anormal do estômago ou cólon no hemitorax esquerdo, usando-se de preferência contrastes iodados, pelo risco da presença de perfuração de vísceras ocas e peritonite química intensa no extravasamento de bário2,23.
O lavado peritoneal diagnóstico realizado em paciente com um hemitorax drenado com saída de líquido do lavado pelo dreno, confirma o diagnóstico de hérnia diafragmática8,33, porém a taxa de lavado peritoneal falso-negativo em casos de hérnia diafragmática é relatada entre 25% e 40%, tendo como possíveis causas a hemorragia contida na retrocavidade dos epíploons por lesão diafragmática posterior esquerda, hemorragia seletiva para dentro da cavidade torácica ou tamponamento imediato do sangramento pela herniação de vísceras1,7,8,10. Na maioria dos casos, a positividade do lavado peritoneal se deve a presença de lesões intra-abdominais associadas

LESÕES ASSOCIADAS
O reconhecimento da ruptura diafragmática é importante pela frequência e gravidade das lesões associadas38.
Devido à grande energia cinética necessária para produzir lesão diafragmática em traumas contusos, é muito freqüente a presença de lesões associadas (72% a 95%)3,6,38, principalmente de baço e fígado em até 25% (no tratamento conservador não-operatório destes órgãos, a lesão diafragmática pode passar despercebida)8, mas também de traumatismo cranioencefálico, fraturas de bacia (40% a 55%) e dos membros3,6,8,16,38. A associação entre lesão diafragmática e fratura pélvica envolve a força maciça necessária para romper o anel pélvico com o súbito e drástico aumento na pressão intra-abdominal, que é transmitida às cúpulas frênicas, causando ou contribuindo para a ruptura do diafragma16.
Em hérnias diafragmáticas do lado direito é maior o número e a gravidade das lesões associadas responsáveis por muitas das complicações. Em cerca de 3% a 10% dos casos, ocorre lesão da aorta torácica, particularmente em lesões do lado direito7.
Nos casos de ferimentos penetrantes, cerca de 66% dos pacientes com trauma diafragmático têm lesões associadas, mais comumente do pulmão e da pleura, resultando em hemotórax ou pneumotórax5. No abdome, os órgãos mais lesados são o baço (24% a 36%), o fígado (23% a 29%) e o cólon (17%)5.


TRAUMATISMO DE URETRA
A uretra masculina é anatomicamente dividida em: prostática, membranosa, bulbar e peniana. As duas primeiras constituem a uretra posterior e as duas últimas, a porção anterior. Os traumatismos da uretra posterior são os que ocorrem do diafragma urogenital para cima e as lesões da uretra anterior, abaixo do diafragma urogenital.
Traumatismo da Uretra Anterior
A ruptura da uretra anterior geralmente acontece por contusões no períneo. A uretra bulbar é esmagada contra o ramo isquiopubiano como resultado de “uma queda a cavaleiro”, ou seja, a queda com as pernas abertas sobre um objeto contuso, tipicamente a barra da bicicleta, cerca ou muro. Outras causas são os chutes sofridos em região perineal ou peniana. Fratura dos ossos da pelve não está geralmente presente. As lesões penetrantes da uretra anterior ocorrem nos empalamentos, tiros e lesões por objetos pontiagudos. Costumam acompanhar as lesões do pênis, como nos esmagamentos, amputações e fraturas. As lesões iatrogênicas da uretra anterior ocorrem por pouca lubrificação da uretra durante a sondagem vesical, pelo enchimento do balão da sonda de Foley na uretra bulbar, durante dilatação da uretra ou endoscopia.
sábado, 16 de julho de 2016
TORÇÃO DE CORDÃO ESPERMÁTICO
O quadro agudo de sinais inflamatórios no escroto deve ser considerado uma situação de emergência, exigindo avaliação imediata.
As principais causas de dor e aumento de volume na bolsa escrotal são torção de cordão espermático, torção de apêndice testicular, torção de apêndice epididimário, orquite, epididimite, tumor de testículo, hematocele traumática e edema escrotal idiopático.
A torção do cordão espermático pode ser extravaginal ou intravaginal.
A torção extra- vaginal consiste na rotação do cordão aci- ma da túnica vaginal, geralmente no canal inguinal ou imediatamente após o anel in- guinal externo. Ocorre no período antenatal ou no período neonatal, com aumento de vo- lume, rubor e endurecimento escrotal que parece não provocar dor. A exploração é executada por inguinotomia devido à possibilidade de torção no canal inguinal ou da presença de outras patologias, como hérnia. Se a torção for confirmada, a fixação do testículo con- tralateral à parede escrotal deverá ser reali- zada.
As torções intravaginais do cordão esper- mático são bem mais freqüentes que as extravaginais, ocorrendo preferentemente en- tre os 3 e 20 anos de idade. Têm como fator predisponente a inserção alta da túnica vagi- nal no cordão espermático. Tal defeito de in- serção geralmente é bilateral, o que determi- na a fixação do testículo contralateral na pre- sença de torção do cordão.
A sintomatologia clássica é de dor agu- da em bolsa escrotal, seguida de aumento de volume e eritema do hemiescroto. Tal qua- dro pode ser relacionado pelo paciente à exe- cução de exercícios físicos ou traumatismo. Às vezes a dor se inicia durante o sono, acordando o paciente. Pode existir o relato de episódios anteriores semelhantes de dor de curta duração, acompanhados de aumen- to de volume da gônada, sendo tal dor cor- respondente a intermitentes torções com dis- torções espontâneas. Não há hipertermia ou sintomas miccionais. No início do quadro pode-se perceber, à palpação, se a dor se deve à rotação de apên- dice de testículo ou de apêndice epididimário ou à epididimite. A gônada afetada pode ter localização alta no escroto ou ter uma orien- tação transversa anormal. A ausência de re- flexo cremasteriano é um sinal de torção do cordão. Pouco tempo após o início da dor aparecem edema e aumento da consistência das camadas do escroto, dificultando o exa- me. A existência de secreção uretral ou piúria induz ao diagnóstico de epididimite.
Na suspeita de rotação do cordão esper- mático, a exploração cirúrgica imediata deve ser executada. O estudo eco-Doppler da bolsa escrotal tem sido o exame de escolha para a avaliação de patologias agudas e crôni- cas do escroto. A solicitação de estudo eco- Doppler serve para confirmar a ausência de torção quando não se acredita estar indicada cirurgia.
Em crianças menores prefere-se, como via de acesso, uma inguinotomia devido à possi- bilidade de patologia inguinal associada. Em adultos e crianças maiores utiliza-se acesso escrotal — incisões transversas ou na rafe. Após ser desfeita a torção, a cor da gônada é observada. Às vezes está claro que o testí- culo está necrótico, sendo óbvia a retirada do mesmo (orquiectomia). Quando há dúvida sobre a viabilidade da gônada, preconiza-se deixá-la coberta por compressa úmida aque- cida enquanto se faz a fixação do testículo contralateral à parede do escroto com fio fino e inabsorvível. A seguir, reavalia-se o testícu- lo distorcido, observando seu aspecto, eventu- ais pulsações de artérias na túnica albu-gínea e pelo sangramento em pequenas incisões fei- tas com bisturi na gônada. Persistindo a dúvi- da, deve-se manter o testículo, fixando-o à pa- rede escrotal ou colocando-o em uma bolsa subdártica.
As principais causas de dor e aumento de volume na bolsa escrotal são torção de cordão espermático, torção de apêndice testicular, torção de apêndice epididimário, orquite, epididimite, tumor de testículo, hematocele traumática e edema escrotal idiopático.
A torção do cordão espermático pode ser extravaginal ou intravaginal.
A torção extra- vaginal consiste na rotação do cordão aci- ma da túnica vaginal, geralmente no canal inguinal ou imediatamente após o anel in- guinal externo. Ocorre no período antenatal ou no período neonatal, com aumento de vo- lume, rubor e endurecimento escrotal que parece não provocar dor. A exploração é executada por inguinotomia devido à possibilidade de torção no canal inguinal ou da presença de outras patologias, como hérnia. Se a torção for confirmada, a fixação do testículo con- tralateral à parede escrotal deverá ser reali- zada.
As torções intravaginais do cordão esper- mático são bem mais freqüentes que as extravaginais, ocorrendo preferentemente en- tre os 3 e 20 anos de idade. Têm como fator predisponente a inserção alta da túnica vagi- nal no cordão espermático. Tal defeito de in- serção geralmente é bilateral, o que determi- na a fixação do testículo contralateral na pre- sença de torção do cordão.
A sintomatologia clássica é de dor agu- da em bolsa escrotal, seguida de aumento de volume e eritema do hemiescroto. Tal qua- dro pode ser relacionado pelo paciente à exe- cução de exercícios físicos ou traumatismo. Às vezes a dor se inicia durante o sono, acordando o paciente. Pode existir o relato de episódios anteriores semelhantes de dor de curta duração, acompanhados de aumen- to de volume da gônada, sendo tal dor cor- respondente a intermitentes torções com dis- torções espontâneas. Não há hipertermia ou sintomas miccionais. No início do quadro pode-se perceber, à palpação, se a dor se deve à rotação de apên- dice de testículo ou de apêndice epididimário ou à epididimite. A gônada afetada pode ter localização alta no escroto ou ter uma orien- tação transversa anormal. A ausência de re- flexo cremasteriano é um sinal de torção do cordão. Pouco tempo após o início da dor aparecem edema e aumento da consistência das camadas do escroto, dificultando o exa- me. A existência de secreção uretral ou piúria induz ao diagnóstico de epididimite.
Na suspeita de rotação do cordão esper- mático, a exploração cirúrgica imediata deve ser executada. O estudo eco-Doppler da bolsa escrotal tem sido o exame de escolha para a avaliação de patologias agudas e crôni- cas do escroto. A solicitação de estudo eco- Doppler serve para confirmar a ausência de torção quando não se acredita estar indicada cirurgia.
Em crianças menores prefere-se, como via de acesso, uma inguinotomia devido à possi- bilidade de patologia inguinal associada. Em adultos e crianças maiores utiliza-se acesso escrotal — incisões transversas ou na rafe. Após ser desfeita a torção, a cor da gônada é observada. Às vezes está claro que o testí- culo está necrótico, sendo óbvia a retirada do mesmo (orquiectomia). Quando há dúvida sobre a viabilidade da gônada, preconiza-se deixá-la coberta por compressa úmida aque- cida enquanto se faz a fixação do testículo contralateral à parede do escroto com fio fino e inabsorvível. A seguir, reavalia-se o testícu- lo distorcido, observando seu aspecto, eventu- ais pulsações de artérias na túnica albu-gínea e pelo sangramento em pequenas incisões fei- tas com bisturi na gônada. Persistindo a dúvi- da, deve-se manter o testículo, fixando-o à pa- rede escrotal ou colocando-o em uma bolsa subdártica.
No paciente cujo testículo torcido foi pre- servado e que posteriormente desenvolveu atrofia, orquiectomia e colocação de prótese testicular estão indicadas.
Lesão Renal
Há várias classificações das lesões traumáticas de rim. Uma das classificações divide-os em lesões menores e maiores. As lesões menores correspondem a 85% dos casos de traumatismo renal e compreendem: •
Laceração mínima (córtex renal). •
Contusão (sem lesão do parênquima, avaliação por imagem normal). •
Laceração menor (córtex, medular, cápsula renal).
As lesões maiores representam 15% dos casos e compreendem: •
Laceração maior (córtex, medular, via excretora, cápsula renal).
Fratura renal (múltiplas lacerações menores e maiores). •
Lesões do pedículo
Lesões mínimas como contusões ou pequenas lacerações do parênquima têm resolução espontânea e devem ser tratadas com repouso no leito e medicação sintomática. A deambulação só será autorizada quando cessar a hematúria macroscópica. As lesões maiores estão comumente associadas com hematomas intra e perirrenais e extravasamento de urina. Quando secundárias a traumatismo fechado geram dúvidas quanto ao seu tratamento inicial, se cirúrgico ou somente observação. Pacientes com estado geral preservado, estáveis hemodinamicamente, devem ser mantidos em repouso até o clareamento da urina. Antibiótico de largo espectro deve ser administrado e, se necessário, devem ser realizadas transfusões sangüíneas.
São indicações para exploração cirúrgica: •
Sangramento incontrolável. •
Lesões do pedículo renal. •
Presença de tecido renal não viável. •
Extravasamento urinário significativo. •
Ferimentos penetrantes (abertos).
A correção da lesão renal deve obedecer aos seguintes princípios: •
Desbridamento do tecido desvitalizado. •
Hemostasia rigorosa. •
Sutura impermeável do sistema coletor. •
Evitar espaço morto. •
Drenagem da loja renal.
O tratamento cirúrgico da lesão renal é feito por via transperitoneal através de incisão mediana xifopúbica.
Laceração mínima (córtex renal). •
Contusão (sem lesão do parênquima, avaliação por imagem normal). •
Laceração menor (córtex, medular, cápsula renal).
As lesões maiores representam 15% dos casos e compreendem: •
Laceração maior (córtex, medular, via excretora, cápsula renal).
Fratura renal (múltiplas lacerações menores e maiores). •
Lesões do pedículo
Lesões mínimas como contusões ou pequenas lacerações do parênquima têm resolução espontânea e devem ser tratadas com repouso no leito e medicação sintomática. A deambulação só será autorizada quando cessar a hematúria macroscópica. As lesões maiores estão comumente associadas com hematomas intra e perirrenais e extravasamento de urina. Quando secundárias a traumatismo fechado geram dúvidas quanto ao seu tratamento inicial, se cirúrgico ou somente observação. Pacientes com estado geral preservado, estáveis hemodinamicamente, devem ser mantidos em repouso até o clareamento da urina. Antibiótico de largo espectro deve ser administrado e, se necessário, devem ser realizadas transfusões sangüíneas.
São indicações para exploração cirúrgica: •
Sangramento incontrolável. •
Lesões do pedículo renal. •
Presença de tecido renal não viável. •
Extravasamento urinário significativo. •
Ferimentos penetrantes (abertos).
A correção da lesão renal deve obedecer aos seguintes princípios: •
Desbridamento do tecido desvitalizado. •
Hemostasia rigorosa. •
Sutura impermeável do sistema coletor. •
Evitar espaço morto. •
Drenagem da loja renal.
O tratamento cirúrgico da lesão renal é feito por via transperitoneal através de incisão mediana xifopúbica.
Esta abordagem permite a correção de lesões associadas de órgãos intracavitários, o controle do pedículo renal antes da abertura da fáscia de Gerota e a verificação in situ do rim contralateral. Tal verificação é de suma importância quando a instabilidade hemodinâmica do traumatizado impede o estudo radiológico antes da cirurgia.
O controle das artérias renais, através da incisão do peritônio posterior, sobre a aorta antes da abertura da fáscia de Gerota, propicia uma taxa menor de nefrectomias. O parênquima lesado deve ser desbridado, e as lacerações graves de um dos pólos indica nefrectomia parcial. A abertura do sistema coletor deve ser reparada com sutura de categute cromado ou ácido poliglicólico (4 ou 5 zeros).
Nas reconstruções da via excretora — cálices, barcinete ou ureter — a drenagem deve ser realizada por nefrostomia ou por cateter ureteral do tipo duplo J ou similar.
A ligadura de vaso intraparenquimatoso é realizada com pontos de fios categute cromado, ácido poliglicólico ou polidiaxone (4 zeros).
Para evitar espaço morto, as bordas da lesão são reaproximadas sempre que possível com sutura de categute cromado 3 zeros, interessando também a cápsula renal. Se as bordas do ferimento forem muito distantes é aconselhável o fechamento da lesão com pontos separados de categute cromado 2 zeros, utilizando-se pequenos coxins de gordura sob os pontos e preenchendo o espaço morto com um retalho de omento ou gordura perirrenal.
Após a correção da lesão renal, a fáscia de Gerota é reaproximada e é introduzida drenagem por drenos de Penrose ou de sucção. Extensas fragmentações do parênquima dificilmente podem ser tratadas de outra maneira que não a nefrectomia.
São complicações do traumatismo renal: hemorragia, fístula urinária, urinoma, pseudocisto, abscesso, atrofia renal, fístula arterio-venosa e hipertensão arterial.
segunda-feira, 11 de julho de 2016
Anatomia do estômago
ARTÉRIAS
O suprimento sanguíneo para o estômago provém da artéria celíaca (tronco celiaco).
Existem quatro grandes artérias:
as artérias gástricas esquerda e direita, ao longo da curvatura menor,
as artérias gastroepiplóicas esquerda e direita, ao longo da curvatura maior
SUPLEMENTAR: As artérias frênicas inferiores e artérias gástricas curtas a partir do baço: uma quantidade substancial de sangue pode ser suprida ao estômago proximal.
1) A maior artéria para o estômago é a artéria gástrica esquerda,
2) A artéria gástrica direita provém da:
artéria hepática
artéria gastroduodenal
3) a artéria gastroepiplóica esquerda origina-se da artéria esplénica
4) a gastroepiplóica direita origina-se da artéria gastroduodenal.
Existe uma extensa conexão anastomótica entre estes dois grandes vasos.
Na maioria dos casos, o estômago sobreviverá se três ou quatro artérias forem ligadas, contando que as arcadas ao longo das curvaturas menor e maior não sejam ligadas.
O suprimento sanguíneo para o estômago provém da artéria celíaca (tronco celiaco).
Existem quatro grandes artérias:
as artérias gástricas esquerda e direita, ao longo da curvatura menor,
as artérias gastroepiplóicas esquerda e direita, ao longo da curvatura maior
SUPLEMENTAR: As artérias frênicas inferiores e artérias gástricas curtas a partir do baço: uma quantidade substancial de sangue pode ser suprida ao estômago proximal.
1) A maior artéria para o estômago é a artéria gástrica esquerda,
2) A artéria gástrica direita provém da:
artéria hepática
artéria gastroduodenal
3) a artéria gastroepiplóica esquerda origina-se da artéria esplénica
4) a gastroepiplóica direita origina-se da artéria gastroduodenal.
Existe uma extensa conexão anastomótica entre estes dois grandes vasos.
Na maioria dos casos, o estômago sobreviverá se três ou quatro artérias forem ligadas, contando que as arcadas ao longo das curvaturas menor e maior não sejam ligadas.
INERVAÇÃO
É tanto parassimpática, através do vago, quanto simpática, através do plexo celíaco.
O nervo vago origina-se no núcleo vago no assoalho do quarto ventrículo e atravessa o pescoço na bainha carotídea para penetrar no mediastino, onde ele se divide em vários ramos ao redor do esôfago.
Estes ramos coalescem acima do hiato esofagiano para formarem os nervos vago esquerdo e direito. No entanto, não é incomum encontrar mais de dois troncos vagais no esôfago distal.
Na junção GE, o vago esquerdo é anterior e o vago direito é posterior (E-A-D-P, mnemónico).
Inervação vagai do estômago. A linha de seção para a vagotomia troncular é mostrada e está acima dos ramos hepático e celíaco dos nervos vagos esquerdo e direito, respectivamente. A linha de secção para a vagotomia seletiva é mostrada, e ocorre abaixo dos ramos hepáticos e celíacos
Conforme mostrado, o vago esquerdo dá origem ao ramo hepático para o fígado e, então, continua ao longo da curvatura menor como o nervo anterior de Latarjet.
O nervo "criminoso" de Grassi é o primeiro ramo do nervo vago direito ou posterior, e é reconhecido como a etiologia potencial das úlceras recorrentes quando não seccionado dividido.
O nervo direito também dá um ramo para o plexo celiaco e, então, continua posteriormente ao longo da curvatura menor.
TIPOS DE VAGOTOMIAS
a vagotomia troncular é executada acima dos ramos celíacos e, RESPETIVAMENTE, hepáticos do vago, a vagotomia seletiva é realizada abaixo destes
a vagotomia superseletiva é realizada seccionando-se a pata de ganso que inerva o estômago proximal enquanto se preserva a inervação das partes antral e pilórica do estômago.
A maioria (>90%) das fibras vagais é aferente, carreando estímulos do intestino para o cérebro.
As fibras vagais eferentes originam-se nos núcleos dorsais do bulbo e fazem sinapses com os neuronios nos plexos mioentéricos e submucosos. Estes neuronios utilizam acetilcolina como seu neurotransmissor e influenciam na função motora gástrica e na secreção gástrica.
Em contraste, o suprimento nervoso simpático provém de T5 a T10, cursando no nervo esplâncnico para o gânglio celíaco. As fibras pós-ganglionares fazem, então, um trajeto junto com o sistema arterial para inervar o estômago.
O sistema nervoso intrínseco ou entérico do estômago consiste em neurônios nos plexos neuronais de Auerbach e de Meissner, neurônios colinérgicos, serotonérgicos e peptidérgicos. A função destes neurônios permanece pouco compreendida.
ESTRUTURA HISTOLOGICA DO ESTOMAGO
1. Exceto por uma pequena área posterior na cárdia proximal e no antro pilórico distal, o estômago é revestido pelo peritônio.
O peritônio forma a serosa, a camada mais externa do estômago.
2. Abaixo dele está uma muscular própria, mais espessa, ou muscular externa, que é composta de três camadas de músculos lisos.
A camada média de múscuIo liso é circular, e é a única camada muscular completa da parede muscular. No piloro, esta camada muscular média circular torna-se progressivamente mais espessa e funciona como um verdadeiro esfíncter anatómico.
A camada muscular externa é longitudinal e contínua com a camada externa do músculo liso esofagiano longitudinal. Dentro das camadas da muscular externa e media encontra-se um rico plexo de nervos autonômicos e de gânglios, denominado plexo mioentérico de Auerbach.
3) A submucosa:
- entre a muscular externa e a mucosa
- camada de tecido conjuntivo rica em colágeno, que é a camada mais resistente da parede gástrica.
- contém a rica rede anastomótica de vasos sanguíneos e de linfáticos e o plexo de Meissner de nervos autonômicos.
5) A mucosa:
- epitélio superficial
- lâmina própria pequena camada de tecido conjuntivo e contém capilares, vasos, linfáticos e nervos necessários para o suporte da superfície epitelial
- muscular da mucosa
responsável pelas rugas que ampliam enormemente a área da superfície epitelial
demarca os limites microscópicos para o carcinoma gástrico invasivo e não-invasivo
Organização Glandular Gástrica
A mucosa gástrica consiste em um epitélio glandular colunar.
As funções das glândulas e as células que revestem as glândulas variam de acordo com a região do estômago na qual elas são encontradas.
As células endócrinas, como as células da gastrina (G) ou da somatostatina (D), podem ser abertas ou fechadas:
o tipo aberto:
- têm as suas microvilosidades nas membranas apicais,
- um contato direto com os conteúdos gástricos.
- as microvilosidades, provavelmente, possuem sensores químicos e de pH que sinalizam à célula para secretar os seus peptídios pré-armazenados.
o tipo fechado não possuem microvilosidades em contato com o lúmen gástrico.
No antro, há células G e células D que são do tipo aberto. As celulas D secretam somatostatina.
Por outro lado, as células D localizadas no fundo/campo do estômago são do tipo fechado e estão em contato direto com as células parietais secretoras de ácido.
Na cárdia, as mucosas são arranjadas em glândulas ramificadas que primariamente secretam muco, e as criptas são curtas. No fundo e no corpo, as glândulas são mais tubulares e as criptas são mais longas. No antro, as glândulas são mais ramificadas.
As extremidades luminais das glândulas gástricas e das criptas são revestidas por células epiteliais de superfície secretoras de muco, que se estendem ao longo do colo das glândulas por distâncias variáveis. Na cárdia, as glândulas são predominantemente secretoras de muco. No corpo, as glândulas são revestidas a partir do colo até a base principalmente com células parietais e principais. Existem umas poucas células parietais no fundo e no antro proximal, mas nenhuma na cárdia ou no antro pré-pilórico. Os espécimes de biopsia retirados do estômago demonstraram que as células parietais são responsáveis por 13% das células epiteliais, enquanto as células principais são responsáveis por 44%; as células mucosas são responsáveis por 40% e as células endócrinas são responsáveis por y/a.
Assinar:
Comentários (Atom)



























